Our Job Opportunities
Why join CellCarta?
If you are passionate about science, strive for new challenges in a fast-pace environment, and ready to work in a highly collaborative organization, join CellCarta and help shape the future of precision medicine.
We are a leading global contract research organization (CRO) laboratory with headquarters in Canada. Our mission is to map precision medicine by providing comprehensive testing solutions and biomarker research to the top global pharmaceuticals and biotech companies. We are committed to providing superior science through proactive partnerships with our clients.
Join our multidisciplinary CRO team and help shape the future of data-driven drug development.
A scientific team that upholds the highest quality standards
More than your traditional CRO, we have a scientist-to-scientist approach and our culture is one of flexibility, accessibility, and service excellence. We are looking for science enthusiasts driven by innovation and eager to join a diversified team of scientists.
At CellCarta we are committed to giving our team the very best. Join us as we continue to expand internationally and be part of the future of precision medicine.
Our projects span therapeutic areas like oncology, cell therapy, infectious diseases, and neuroscience – giving our teams exposure to the frontlines of translational medicine and scientific innovation.
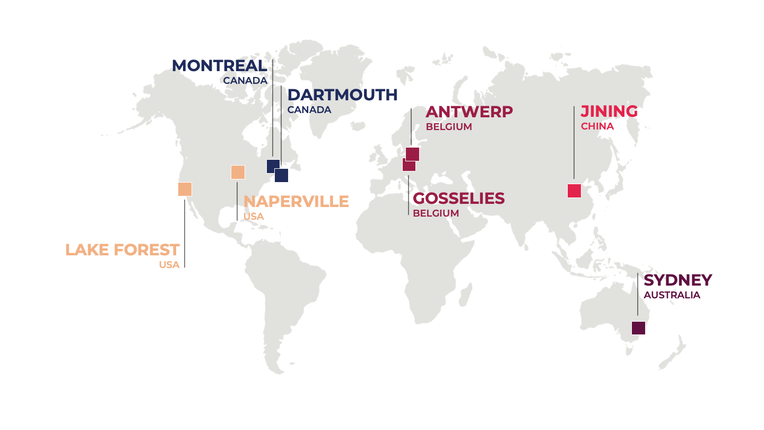
Our Locations:
GO FURTHER
- Exciting and superior scientific environment with a multidisciplinary team of experts
- Multiple growth opportunities and career development plan
MOVE WITH CONFIDENCE
- The assurance that comes from working for an established leader
- The reputation of a scientific team that upholds the highest quality standards
MAKE A DIFFERENCE
- The opportunity to significantly contribute to the next generation of life-changing drugs in precision medicine
- Join a global CRO where your expertise shapes the science behind biomarker assay development and validation – central to advancing precision medicine and bringing therapies to market.
Our Values:
- Collaboration
- Customer Excellence
- Respect
- Trust & Accountability
Recruitment fraud alert:
At CellCarta we are committed to providing a secure and transparent hiring process, and we want to ensure that you can confidently explore career opportunities with us.
Unfortunately, we have been made aware of recruitment fraud involving scammers posting fraudulent job openings, conducting interviews while posing as legitimate CellCarta employees, and sending fraudulent job offers, with the intent to obtain personal information or money from applicants.
How to identify recruitment fraud:
- CellCarta will never request an interview through instant messaging applications nor by text messaging.
- Initial interviews with CellCarta recruiters are conducted by phone and all hiring manager interviews are conducted either through Microsoft Teams or in person.
- CellCarta will never ask for any fees or payments from candidates for any purpose during or after the recruitment process. If you’re asked to pay any money to secure a position, it is likely a scam. If you suspect fraudulent activity, please contact your local authorities.